Ульяновская область
Муниципальный этап Всероссийской олимпиады школьников по химии 2010-2011
Инструкция по выполнению заданий
На выполнение 6 заданий олимпиады отводится 4 часа (240 мин). Каждое из 6 заданий включает условие и вопросы. Прежде чем отвечать на вопросы, внимательно прочитайте условия задания. Постарайтесь ответить на все заданные вопросы. Все задания оцениваются примерно одинаковым количеством баллов, но неравноценны по трудности. Начинайте выполнение заданий с самых лёгких, постепенно переходя к более трудным. При выполнении заданий можно пользоваться периодической системой Д.И.Менделеева, таблицей растворимости, электрохимическим рядом напряжений металлов, калькулятором. Желаем успеха!
8 класс
Задание 8-1. НЕИЗВЕСТНОЕ ВЕЩЕСТВО
Это вещество:
- встречается в природе в растворенном виде или в виде полупрозрачных кристаллов;
- содержится практически в любом образце жидкой воды на Земле (кроме дождевой)
- содержит в своем составе металл, практически все соли которого хорошо растворимы в воде; этот металл отвечает за межклеточный обмен органических веществ;
- содержит неметалл, название которого указывает на его цвет;
- в больших количествах поглощается человеком во все периоды его жизни, хотя врачи постоянно напоминают о его пагубном влиянии на наше здоровье;
- в древности было мерилом богатства человека, а теперь его может приобрести каждый.
Вопросы:
1) Запишите формулу вещества и дайте его химическое название
2) Вычислите массовую долю металла в этом веществе (%).
3) Рассчитайте массы химических элементов, содержащихся в одной упаковке (1 кг), этого вещества.
4) В результате реакции, каких простых веществ может образоваться это вещество? Составьте уравнение соответствующей химической реакции.
5) Опишите, как это вещество можно выделить из водного раствора?
6) Сколько г этого вещества можно выделить из 120 г его 10%-ного раствора?
Задача 8-2. ВЕЩЕСТВА И ХИМИЧЕСКИЕ ЭЛЕМЕНТЫ
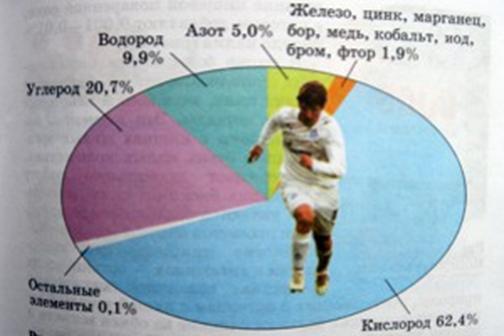
Фотография полузащитника сборной России по футболу и лондонского «Арсенала» Андрея Аршавина попала на страницы одного из учебников по химии для 9 класса.
Вопросы:
1) О чем идёт речь на представленной диаграмме о веществах или химических элементах?
2) Рассчитайте массу кислорода в организме футболиста, если масса Андрея составляет 70 кг.
3) Сколько моль и сколько атомов кислорода содержит организм футболиста?
4) Приведите пример вещества, в состав которого входит элемент кислород, и рассчитайте его массовую долю.
5) Приведите пример смеси, в состав которой входит вещество кислород и оцените его объёмную долю в этой смеси.
6) Приведите уравнение химической реакции водорода с кислородом. Сколько г водорода вступило в реакцию, если масса прореагировавшего кислорода составила 8 г?
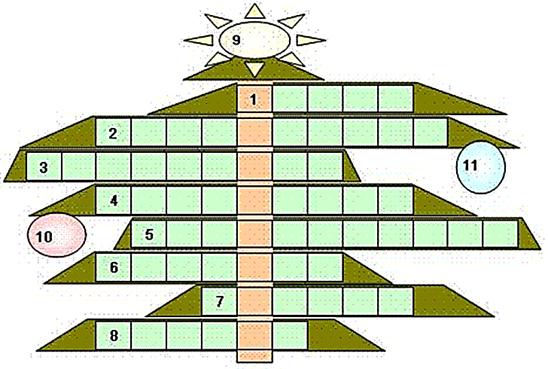
Задание 8-3. ХИМИЧЕСКИЙ КРОССВОРД
Волька приготовил кроссворд к новогоднему химическому вечеру. Долго бился над ним старик Хоттабыч, но так ничего и не получилось. Сможешь ли ты помочь ему ответить на эти вопросы? А Хоттабыч подскажет, как заполнить центральные выделенные клеточки.
Вопросы:
1) Наука, изучающая вещества и их превращения.
2) Тип реакции, с помощью которой получают кислород в лаборатории.
3) Его используют, чтобы отличить кислоту от щелочи.
4) Устройство для нагревания пробирок.
5) Реакцию ускоряет, а сам не расходуется.
6) Латинское название элемента свинец
7) Элемент, в названии которого встречаются два существа, а формула оксида – Э2О5.
8) Растворимый гидроксид активного металла.
А теперь помоги старику Хоттабычу повесить украшения на ёлку. Впишите символ химического элемента в ёлочное украшение.
9) Символ элемента, сначала открытого на солнце, а теперь используемого для надувания шариков.
10) Символ элемента, предсказанного Д.И. Менделеевым, на внешнем уровне – 4 электрона.
11) Символ элемента, который в виде простого вещества является основной частью атмосферы.
Задание 8-4. АЛХИМИЯ И ГЁТЕ
Алхимики не знали состава используемых веществ, не умели их анализировать и химические взаимодействия записывали словами. Вещества, участвующие в химических реакциях они называли, не руководствуясь никакими правилами, и поэтому понять, что они делали, было очень трудно. Гёте в «Фаусте» дал пример записи алхимической процедуры:
«Являлся красный лев – и был он женихом,
И в тёплой жидкости они его венчали
С прекрасной лилией, и грели их огнём,
И из сосуда их в сосуд перемещали…»
Зная особое пристрастие алхимиков к соединениям ртути, можно предположить, что «Красный лев» – это красный оксид ртути HgO, а «прекрасная лилия» – хлороводородная кислота HCl.
Вопросы:
1) Составьте уравнение химической реакции между «красным львом» и «прекрасной лилией».
2) Сколько г «красного льва» может прореагировать с 100 г 36,5%-ного раствора «прекрасной лилии»?
3) Кроме ртути людям с древности было известно ещё 6 металлов. Назовите любые 3 металла (кроме ртути), известные людям с древности.
Задание 8-5. ЯДЫ И ОТРАВЛЕНИЯ
А) Известно, что по официальной версии Наполеон умер от рака желудка. Спустя 140 лет ученые пришли к выводу, что, скорее всего он был отравлен ядовитыми соединениями элемента Х. Вероятно, Наполеону длительное время в пищу подмешивали вещество Х2О3 в малых дозах.
Б) 17 декабря 1916 года князь Феликс Юсупов с сообщниками пытался отравить приближенного к семье последнего российского императора, одну из самых одиозных фигур российской истории – Григория Распутина, добавив яд «Y» в пирожные. Однако яд не подействовал, и Распутин был убит 11 выстрелами. Проведённый анализ позволил определить состав яда. Он состоял из калия – 60%, углерода – 18,46% и азота – 21,54%.
В) Есть много людей, обожающих париться в бане. Однако в русской бане не исключена угроза отравления угарным газом. Признаки отравления угарным газом детально описаны: сначала сильное головокружение, необыкновенная бледность лица, у некоторых бывает рвота, потом глубокий обморок, а при продолжительном воздействии газа – летальный исход. Чтобы избежать этой опасности, необходимо придерживаться следующих правил: когда баня истоплена и достаточно уже прогрета, надо тщательно перемешать угли в топке, чтобы не осталось даже маленькой тлеющей головешки. Если в топке имеются большие тлеющие головешки, их следует оттуда убрать и погасить в ведре. Из поддувала печки также нужно все выгрести, так как там могут находиться долго тлеющие угли.
Вопросы:
1) Установите элемент «Х», если известно, что его массовая доля в оксиде составляет 75,7%.
2) К металлам или неметаллам относится элемент «Х»?
3) Каким веществом пытались отравили Распутина?
4) Выведите формулу вещества, которым пытались отравить Распутина.
5) Запишите формулу угарного газа
6) Выведите формулу угарного газа, если известно, что он относится к оксидам, а массовая доля углерода в нём составляет 42,86%.
Задание 8-6. ГАЗЫ И ИХ СВОЙСТВА
В четыре пробирки, наполненные газами, внесли поочередно тлеющую лучинку. В первой пробирке произошел глухой хлопок, во второй хлопок со свистом, в третьей пробирке лучинка воспламенилась, а в четвертой погасла.
Вопросы:
1) Определите, какие газы находились в каждой из пробирок, если известно, что это были (азот, кислород, смесь водорода с воздухом, водород)?
2) Что такое гремучий газ?
3) Составьте уравнения реакций угля с избытком и недостатком кислорода.
К какому классу оксидов, относятся полученные вещества?







Интресные задания)